CONFIGURACIÓN ELECTRÓNICA
CONFIGURACIÓN ELECTRÓNICA.
La configuración electrónica de un elemento es una
representación de la estructura electrónica del átomo. Nos muestra dónde
se ubican los electrones en los distintos niveles y subniveles energéticos y
orbitales que rodean el núcleo atómico.
Para los 118 elementos confirmados, los electrones se
posicionan en siete niveles energéticos o capas. El primero, 1, es el de menor
energía y más cercano al núcleo atómico. Conforme aumenta el nivel energético,
los electrones tendrán más energía, pero estarán más alejados del núcleo.
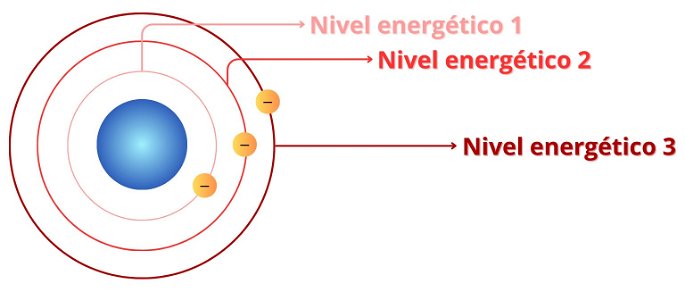
Representación simplificada de los tres primeros niveles
energéticos.
Dentro de cada nivel hay subniveles o subcapas que albergan
electrones. Dependiendo del subnivel, podrá contener uno o más pares de
electrones:
- Subnivel
s: es el subnivel más pequeño. Contiene un orbital, por lo que puede
albergar un par de electrones, con un total de 2.
- Subnivel
p: contiene tres orbitales, por lo que puede albergar tres pares de
electrones, con un total de 6.
- Subnivel
d: contiene cinco orbitales, por lo que puede albergar cinco pares de
electrones, con un total de 10.
- Subnivel
f: contiene siete orbitales, por lo que puede albergar siete pares de
electrones, con un total de 14.
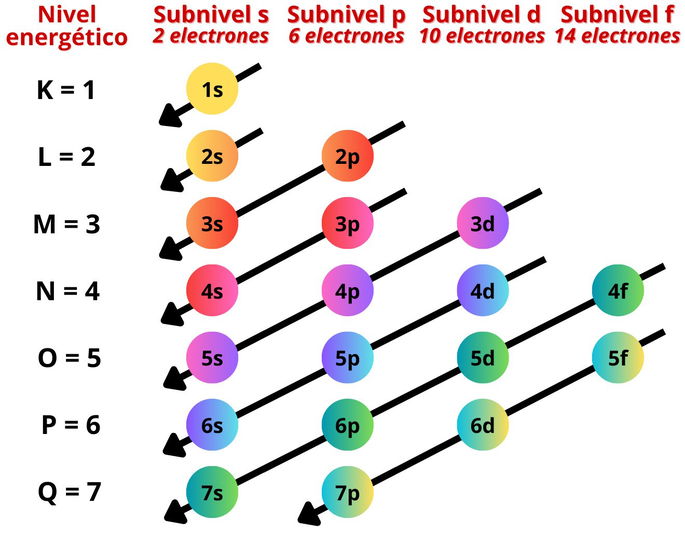
El diagrama está basado en el principio de Aufbau y la regla
de ordenación de Madelung. En conjunto, ambos establecen que un átomo primero
llena los niveles energéticos más bajos y subniveles más pequeños. Es decir,
primero se llenará el nivel 1 y subnivel s, o 1s, antes del resto. Luego, los
electrones ocuparán los subniveles 2s, 2p, 3s, 3p, 4s, etc.
Para ilustrar cuántos electrones hay en un subnivel, nos
servimos del superíndice. Por ejemplo, si el subnivel 2p de un átomo contiene
cinco electrones, lo representamos como 2p5. De esta forma, la
configuración electrónica de un átomo nos informa tanto de la ubicación de
los electrones como de la cantidad.
Para terminar, podemos emplear la notación de Kernel para
simplificar configuraciones electrónicas usando los gases nobles como
referencia. Por ejemplo, la configuración del sodio se escribe como 1s2 2s2 2p6 3s1 o
[Ne] 3s1, tomando como referencia el neón.
Ejemplos de configuración electrónica
Configuración electrónica del nitrógeno
El nitrógeno es un elemento que, en su isótopo más estable y
abundante, contiene 7 electrones y protones. Al haber más de dos
electrones, eso implica que el primer nivel se llenará completamente. Por lo
tanto, empezamos con 1s2, o sea, dos electrones emparejados.
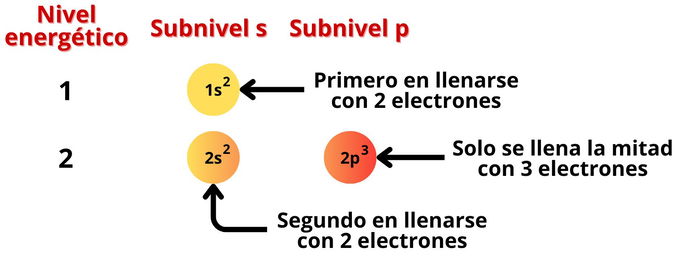
Faltan 5 electrones por ubicar. Según el diagrama, el
siguiente nivel y subnivel es el 2s. Como siguen quedando más de dos
electrones, este nivel también se llena y obtenemos 2s2. Los
últimos 3 electrones se colocan en el subnivel 2p, dando lugar a 2p3.
En resumen, la configuración electrónica del nitrógeno
es 1s2 2s2 2p3, o [He] 2s2 2p3 según
la notación de Kernel.
Configuración electrónica del calcio
El calcio es un elemento que posee 20 electrones y
protones, por lo que es más pesado que el nitrógeno. Si partimos de la
configuración electrónica anterior, vemos que podemos llenar los
subniveles 1s2 2s2 2p6.
Los 10 electrones restantes se repartirán en los próximos
subniveles. Si nos fijamos en el diagrama, vemos que los próximos tres
subniveles son el 3s, 3p y 4s, los cuales suman un total de 10 espacios para
electrones. Por lo tanto, estos subniveles también se llenan, dando lugar
a 3s2 3p6 4s2.
Es decir, la configuración electrónica del calcio es 1s2 2s2 2p6 3s2 3p6 4s2,
o [Ar] 4s2 según la notación de Kernel.
Configuración electrónica del bromo
El bromo contiene 35 electrones, o sea, 15 más que el
calcio. Si miramos el diagrama, el próximo subnivel a llenarse tras completar
la configuración del calcio es el 3d, con espacio para 10 electrones. Hay
electrones de sobra, así que el subnivel se llenará, resultando en 3d10.
Los 5 electrones que quedan se colocan en el siguiente
subnivel, 4p, todos emparejados excepto uno. Entonces, la configuración
electrónica del bromo es 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5,
o [Ar] 4s2 3d10 4p5 según la
notación de Kernel.
Alternativamente, la configuración se escribe como 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p5,
intercambiando 4s2 por 3d10 para tener los
niveles energéticos ordenados de menor a mayor.

Exelente información
ResponderEliminarBuen trabajo 👍🏻
ResponderEliminarBuen trabajo profe
ResponderEliminar